Une équipe de chercheurs américains vient de mettre au point un virus de l’herpès génétiquement modifié capable de détruire les cellules cancéreuses chez des patients atteints de mélanome en impasse thérapeutique. Ce traitement serait sur le point d’être approuvé par les autorités sanitaires américaines.
au sommaire
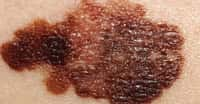
Le mélanome ne représente que 10 % des cancers de la peau, mais c'est de loin la forme la plus grave. En augmentation constante depuis plusieurs décennies, il est en cause dans la plupart des décès par cancers de la peaucancers de la peau.
Le mélanome, un cancer redoutable
Quand il est diagnostiqué tôt, ce cancer est plutôt de bon pronostic. Le traitement se base alors sur un simple retrait chirurgical. En revanche, quand il est diagnostiqué tardivement, ce cancer à fort potentiel métastatiquemétastatique peut s'étendre rapidement à d'autres organes, nécessitant, en plus de la chirurgie, différents traitements complémentaires (curage ganglionnaire, immunothérapie, radiothérapie, chimiothérapiechimiothérapie...) qui ne suffisent toujours pas pour en venir à bout.
Le mélanome serait à l'origine de 150 000 décès chaque année en Europe. En France, selon l'Institut national du cancer (Inca), près de 18 000 personnes étaient touchées par ce cancer en 2023, causant 1 980 décès. C'est l'un des cancers dont l'incidenceincidence et la mortalité ont significativement augmenté depuis 40 ans.
Recherche traitement désespérément
C'est pour trouver des solutions quand plus aucun traitement ne marche que les scientifiques se sont intéressés aux virusvirus de l'herpèsherpès. Ça peut paraître étonnant, mais on sait depuis plus d'un siècle que les infections virales peuvent aider à combattre le cancer.
Problème : injecter des agents infectieux chez quelqu'un déjà éprouvé par la maladie peut s'avérer délicat. C'est pour cette raison que des biologistes ont commencé à modifier génétiquement les virus. Objectif : créer des micro-organismesmicro-organismes capables d'infecter et détruire les cellules cancéreuses et provoquer une réponse immunitaireréponse immunitaire spécifiquement ciblée sur elles, mais sans nuire aux cellules saines.
Un virus capable d’atteindre les tumeurs profondes
L'Herpes simplexsimplex virus (HSV) - le micro-organisme responsable du fameux herpès labial ou génital - a par exemple été modifié pour être capable d'amener les cellules tumorales infectées à libérer un facteur stimulant l'immunitéimmunité et détruisant les cellules cancéreuses.
Ce traitement dit « immunothérapie oncolytique », appelé TT-VEC (ou Imlygic), a été approuvé en Europe et aux États-Unis pour traiter les mélanomes inopérables. Le problème, c'est que l'approbation ne concernait que son injection directement dans les tumeurstumeurs. Or, parfois, les mélanomes avancés présentent des tumeurs profondes, plus difficiles d'accès, et qui ne peuvent donc pas bénéficier de ce traitement.
Régression et même disparition complète des tumeurs
L'équipe du docteur Gino Kim In, de l'Université de Californie du Sud, a repris le virus Herpes simplex et l'a modifié génétiquement pour qu'il soit capable de provoquer la fusionfusion des cellules tumorales et qu'il aide le virus à se propager dans les tumeurs en renforçant la réponse immunitaire. Ce virus - nommé RP1 - a été injecté dans les tumeurs de 140 personnes atteintes de mélanome avancé en impasse thérapeutique (celles-ci avaient reçu en parallèle un traitement appelé nivolumab, destiné à stimuler la réponse immunitaire contre les tumeurs).
Les résultats, présentés début juin au meeting de l'American Society of Clinical Oncology (ASCO), indiquent que chez 30 % des personnes traitées, les tumeurs ont régressé, y compris celles qui n'avaient pas reçu directement l'injection, ce qui indique un effet systémique puissant. Dans la moitié de ces cas, les tumeurs ont complètement disparu.
Une autorisation de mise sur le marché imminente
« Nous sommes très enthousiasmés par ces résultats, se réjouit Gino Kim In. Les autres options thérapeutiques disponibles à ce stade ne sont pas aussi efficaces et ont des effets secondaires plus graves. »
Prochaine étape : attendre les résultats d'un nouvel essai cliniqueessai clinique actuellement en cours, cette fois sur 400 personnes. Mais le RP1 pourrait être approuvé par les autorités sanitaires américaines (FDAFDA) avant la fin de l'essai et obtenir une autorisation de mise sur le marchéautorisation de mise sur le marché (AMM), a confié le médecin au journal New Scientist. « La FDA devrait nous donner sa décision à la fin du mois », leur a-t-il expliqué.



.jpg)